§23 绿色化学实验管(又名:多用实验管)
原创作者:江苏省徐州市科技中学 李 敏
(可以转载,但不能故意抹掉或假冒原创作者,不可剽窃核心内容发表或参赛。)
1 绿色化学实验管组成和工作原理
绿色化学实验管(如图1所示)全由玻璃制造,分为外管、内管和顶塞三部分。外管上有一个小支管,内管中部有一个小孔,内管插入外管里,形成既独立又连通的两个空间,向内放入不同的试剂,就可以简便快速、 无污染地做二氧化碳的四个性质实验、不用加热制取氨气和氯化氢气等实验。
2实验方法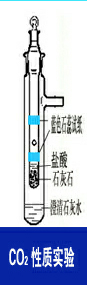
2.1 CO2性质实验:(如图2所示)
向外管注入1~2ml澄清石灰水,在距内管气孔上下约1.5 cm处各缠绕一条湿润的蓝色石蕊试纸,向内管加入几粒石灰石碎块和稀HCI,盖上顶塞,二氧化碳从中部气孔排出,将内管插入外管。片刻石灰水出现白色混浊;随后内管气孔下部一条石蕊试纸先变红色,上部一条试纸后变红色;食指堵住支管口,拔下顶部活塞,插入燃烧的火柴,火柴熄灭。结论:
①通过石蕊试纸变红色,证明二氧化碳是酸性氧化物;
②二氧化碳能使澄清的石灰水变混浊;
③通过石蕊试纸变色顺序说明二氧化碳的密度比空气大;
④二氧化碳不能燃烧,且不支持燃烧。
化学反应方程式:
CaCO3+2HCl(稀) ==CaCl2+CO2↑+H2O
Ca(OH)2 ==CaCO3↓+H2O
H2O +CO2 ==H2CO3
此实验验可让学生从另一角度认识二氧化碳的性质,实验时间在2min左右,教师可采用边实验边让学生练写化学方程式的方法,在课堂教学总结时做该实验,亦可作为探究型实验,生动活泼,方法新颖,定会给教学添写精彩一笔。
2.2 NH3和HCl气体的化合反应:(如图6所示)
向外管里注入0.5mL浓氨水,向内管加入1ml浓盐酸,把内管插入外管里。摇荡一下多用实验管,氨气和氯化氢气体挥发出来,两种气体在管里发生化合反应,生成的白烟充满多用实验管。
化学反应方程式:HCl+NH3== NH4Cl
2.3 不加热快速制氨气:
外管加入5g左右固体NaOH,内管加氯化铵饱和溶液。当溶液滴到固体NaOH上,溶解时放出的热量替代了加热。NH3由支管导出。用加氯化铵溶液的多少控制NH3的产出量。若需大量NH3,可换成浓氨水滴入。此法可以快速制取大量NH3气,且不需加热,简单易行。
化学反应方程式:NaOH+NH4Cl==NaCl+NH3↑+ H2O
2.4不加热快速制HCl气体:
外管加入浓硫酸,内管加浓盐酸,浓盐酸从内管小孔里流到浓硫酸上,浓硫酸密度大沉在下部,浓盐酸密度小浮在上部,初始没有明显反应,稍作振荡,HCl气体迅速生成,从外管上的支管排出。此法是利用浓硫酸的吸水性快速制取大量HCl气体,无需加热。
▲ 注意:实验方法中的1、2适用于教师课堂演示实验;实验方法中的3、4适用于实验教师准备实验。
上篇:§22《燃料电池》H2-O2电池和H2-Cl2电池
下篇:§24制取一氧化碳、氯气等气体时,分液漏斗里的酸液放不下来怎么办?
推荐:“实验误区”应细细研读。
有感想就在“实验论坛”里畅谈

|