§31 Fe(OH)3胶体电泳实验的改进
原创作者:附中大理分校大理新世纪中学 李 铜
(可以转载,但不能故意抹掉或假冒原创作者)
人民教育出版社全日制普通高级中学教科书(必修加选修)第三册第19页讲胶体性质中Fe(OH)3胶体电泳是高中化学中关于胶体性质的一个重要实验。因课本Fe(OH)3胶体电泳实验是采用把电极直接插入胶体内使溶胶被破坏而凝聚析出胶粒,聚集成的颗粒使电极附近的溶胶变成红褐色沉淀,即形成电泳,但现象不明显,笔者通过反复实验改进实验装置和实验方法后实验效果较明显。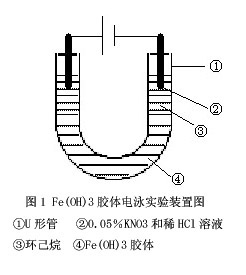
1.实验装置如右图1所示
2.操作步骤及现象
2.1 Fe(OH)3胶体的制备
在100mL煮沸的蒸馏水里滴入10滴FeCl3饱和溶液,冷却至室温,再加入2g尿素,缓慢搅拌,即制得深棕色Fe(OH)3胶体。
2.2 KNO3溶液的配制
将固体KNO3加入到室温的蒸馏水中全部溶解,浓度为0.05%。
2.3 如图1所示安装装置
2.4 操作
2.4.1 在洁净的15×150 mmU形管中加入Fe(OH)3胶体,从U形管底部到液面的高度约6 cm,用滴管吸取环己烷2 mL,分别沿U形管壁交替地缓慢滴入,再沿U形管壁加入4 mL KNO3溶液和稀HCl 5滴,不能搅动胶体,要求上下两层之间有明显的界面。
2.4.2 将石墨电极分别插入 KNO3和稀HCl溶液中约2 cm处。
2.4.3 选用240V高压直流电源,30秒后即可见阴极区0.05%KNO3和稀HCl溶液下面的胶体颜色加深,阳极区胶体颜色变浅,这表明Fe(OH)3溶液中正电荷在外电场作用下向阴极移动。
3.对比实验
3.1 电源,见表一:
表一 电源与完成反应所需要的时间之间的对比
|
电源/V |
12 |
24 |
28 |
100 |
120 |
240 |
|
完成反应所需要的时间/分钟 |
300 |
20 |
15 |
5 |
2 |
0.5 |
3.2 对比分别含有KNO3、NaCl、KBr、KI四种电解质的溶胶在相同实验条件下的电泳速度,实验表明,用KNO3电解质效果最好。因为KNO3中K+和NO3-的迁移率较接近,其导电性较好。见表二:
表二 298.15K时一些离子在无限稀水溶液中的电迁移率
|
正离子 |
K+ |
Na+ |
H+ |
|
×108/m2 s-1 V-1 |
7.62 |
5.20 |
36.20 |
|
负离子 |
Cl- |
Br- |
I- |
NO3- |
OH- |
|
×108/m2 s-1 V-1 |
7.91 |
8.21 |
7.96 |
7.40 |
20.50 |
3.3 在这个实验中选用苯或环己烷的作用是为了防止滴加KNO3溶液时扰动胶体的液
面,使胶体与KNO3溶液保持清晰的界面。笔者为何选用环己烷?见表三:
表三 苯与环己烷性质的对比
|
ρ |
挥发性 |
溶解性 |
毒性 |
|
苯 0.885g/cm3(15℃) |
易 |
难溶于水,易溶于乙醇、乙醚等有机溶剂 |
有毒 |
|
环己烷 0.778g/cm3(20℃) |
难 |
几乎不溶于水,能与乙醇、苯等混合 |
毒性比苯小 |
4.注意事项
4.1 制备Fe(OH)3胶体过程中若产生沉淀,应重做。
4.2 电极不能直接插入胶体中,否则因电解而产生聚沉现象会掩蔽胶体的电泳现象。
4.3 KNO3溶液要稀一些,如果太浓时电泳时间过长,在阴极区易发生凝聚。若其溶液中加入少量的稀HCl,可防止凝聚现象发生。
4.4 环己烷是非电解质,且ρ小于1,所以选环己烷为缓冲剂,便于KNO3与溶剂分层;在Fe(OH)3胶体中加入尿素是为了增大溶胶的ρ,便于KNO3溶液与溶胶分层且尿素是非电解质,不影响溶胶的性质。
5.实验优点
5.1 用以上方法现象明显(无色与有色液差达2cm―4cm)。
5.2 操作简便,符合教学要求。
|